Forskningsprosjekter
Persontilpasset tamoxifenbehandling
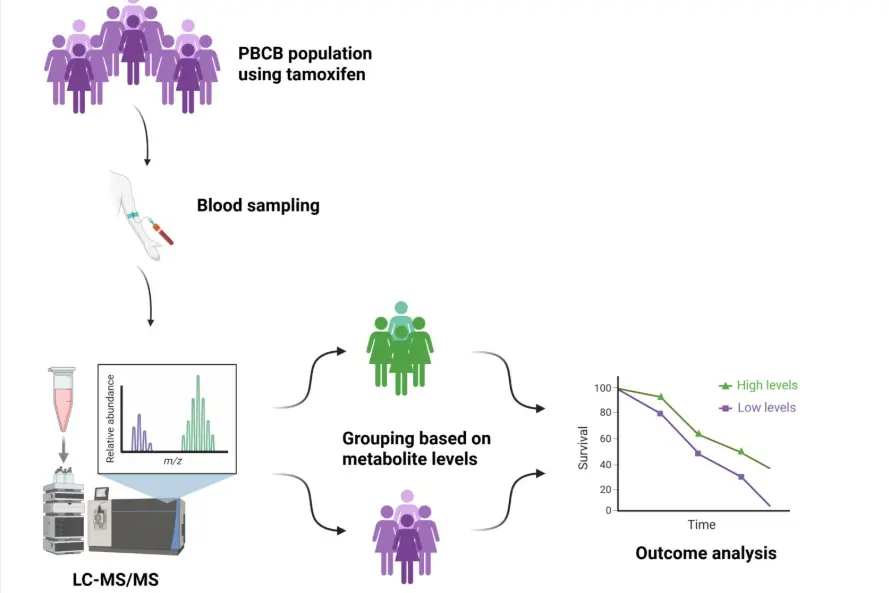
Pasienter med østrogenreseptor positiv tumor utgjør ca. 3/4 av alle brystkrefttilfeller. Hos disse pasientene finner man reseptorer for østrogen i kreftsvulsten, noe som kan utnyttes i behandlingen (såkalt endokrin adjuvant behandling). Pasientene får da antiøstrogen tilleggsbehandling i 5-10 år for å redusere risikoen for tilbakefall. Tamoxifen er et legemiddel som har en sentral rolle i slik antiøstrogen behandling, spesielt for yngre og premenopausale pasienter.
Tamoxifen omsettes ulikt mellom pasienter, og den individuelle (genetisk bestemte) metabolismen av tamoxifen i leveren fører til svært ulike serumnivåer av de aktive formene av tamoxifen. De aktive formene (aktive metabolitter) er 100x mer effektive til å stoppe celledeling av eventuelle gjenværende brystkreftceller etter operasjonen. Dr. Thomas Helland har publisert to studier som indikerte at pasienter som har lave nivåer av aktive tamoxifenmetabolitter trolig har dårligere langtidsoverlevelse enn pasienter som har høyere nivåer. PBCB-materialet vil bli benyttet til validering av dette funnet, når oppfølgingstiden er lang nok. Slike målinger kan eventuelt gi klinikeren et verktøy til å optimalisere den endokrine adjuvante behandlingen ved for eksempel å gi pasienter tilpasset mengde og type antiøstrogen.
Adherence (behandlingsetterlevelse) til antiøstrogenbehandling
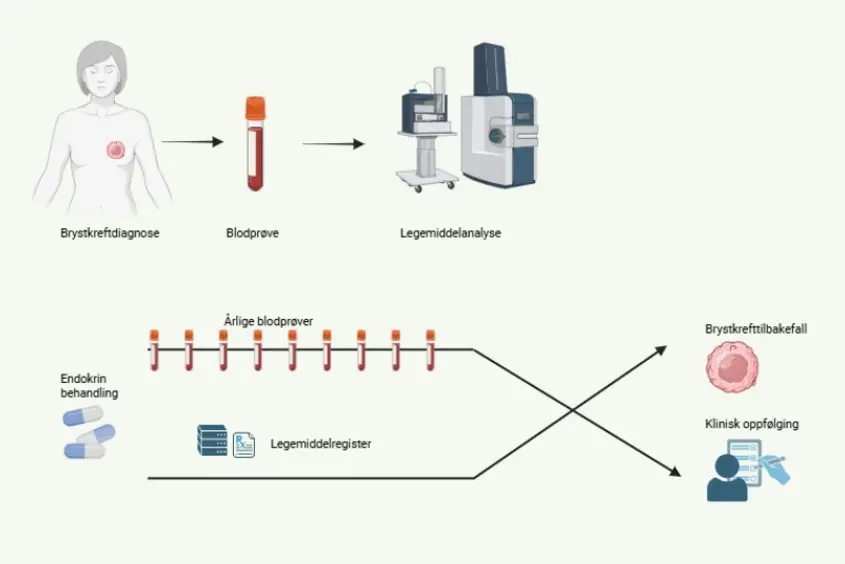
Hele 70 % av brystkreftpasientene har svulster som er blitt avhengige av østrogener for å leve. Derfor er antiøstrogenbehandling en svært effektiv og viktig tilleggsbehandling (adjuvant endokrin behandling) til disse kvinnene. Denne terapiformen består i å ta en østrogenblokkerende tablett daglig i opptil 10 år, og foregår derfor uten tilsyn av helsepersonell. Da anti-østrogenbehandlingen ofte genererer en rekke bivirkninger med redusert livskvalitet, øker dette risikoen for at pasientene selv velger å avslutte behandlingen altfor tidlig. Dette medfører dessverre en økt risiko for tilbakefall av brystkreftsykdom. Identifikasjon av pasienter med høy risiko for å avbryte antiøstrogenbehandlingen vil kunne forbedre oppfølgingen, og øke langtidsoverlevelsen hos disse kvinnene.
I dette prosjektet fokuserer PhD stipendiat Finn Magnus Eliassen på om dårlig behandlingsetterlevelse (adherence; at pasienten faktisk tar medisinen) til endokrin behandling fører til flere tilbakefall og økt dødelighet av brystkreft. Det tas i bruk reseptregisterdata for å vurdere etterlevelse og disse dataene sammenlignes med analyser av blodprøver tatt i samme tidsrom. Den lange oppfølgingstiden i PBCB tillater at man også kan ta høyde for sene tilbakefall, som er en spesiell utfordring med østrogensensitiv brystkreft.
Videre vil vi ta i bruk registrerte PROM data (svar på spørreskjemaene) for å se nærmere på hvordan endokrinbehandling påvirker den selvrapporterte seksuelle helsen til pasientene, og spesielt om dårligere seksuell helse hos denne pasientgruppen fører til dårligere etterlevelse av behandlingen.
Persontilpasset monitorering av brystkreft (PerMoBreCan)
I PerMoBreCan prosjektet er målet å undersøke den kliniske nytteverdien av nye sirkulerende biomarkører ( som for eksempel sirkulerende tumorceller, sirkulerende tumor DNA, metabolitter, ekstracellulære vesikler, proteiner, glykoproteiner og cytokiner fra blod) for tidlig påvisning av et eventuelt systemisk tilbakefall hos brystkreftpasienter slik at ny behandling kan startes tidlig. Prosjektet er organisert i flere delprosjekter som inkluderer undersøkelse av kreftsvulsten, samt de nye aktuelle sirkulerende tumor markørene i blodprøver fra brystkreftpasienter inkludert i PBCB-prosjektet.
Delprosjekt 1: Analyse av brystkreftsvulsten og sirkulerende mikro-RNA fra ekstracellulære vesikler
I dette prosjektet har brystkreftsvulstenes RNA blitt sekvensert for å identifisere nye mikroRNA-profiler som kan skille mellom svulster som er følsomme for adjuvant kjemoterapi og svulster som er resistente. I tillegg vil brystkreftsvulstene bli sjekket for genfeil, spesielt i østrogen reseptor genet og andre kjente kreftgener (onkogener). Også såkalt Ki67-Justert Mitotisk Score (KAMS), som gir et mål på cellesyklus kinetikk av den proliferative populasjon av celler, vil bli vurdert. Sentrosom amplifikasjon (som et mål for svulst heterogenitet og kromosom ustabilitet) vil bli analysert.
Genfeilene i brystkreftsvulstene har også blitt kartlagt, og denne analysen knyttes opp mot analysen av sirkulerende tumor DNA for identifisering av kreft-DNA i blodet som tegn på spredning av kreftsykdommen.
I tillegg vil vi også analysere sirkulerende mikro-RNA fra ekstracellulære vesikler. MikroRNA-profiler fra brystkreftsvulster som er følsomme for adjuvant kjemoterapi vil da bli sammenlignet med profiler fra mer behandlingsresistente svulster. Aktuelle mikro-RNA markører (funnet ved analyser av brystkreftsvulster, og som samsvarer med behandlingsrespons) vil bli analysert for total-RNA isolert fra ekstracellulære vesikler fra høyrisiko- pasienter. Her vil vi se hvorvidt disse mikro-RNAene kan anvendes for behandlingsovervåking, oppfølging og tidlig påvisning av et systemisk tilbakefall. I tillegg til dette undersøkes genuttrykk av bestemte gener i blodplater. Arbeidet utføres av bioinformatiker Marie Austdal ved Avdeling for patologi, Stavanger Universitetssykehus.
Delprosjekt 2: Validering av nye biomarkører for påvisning av tidlig tilbakefall hos brystkreftpasienter
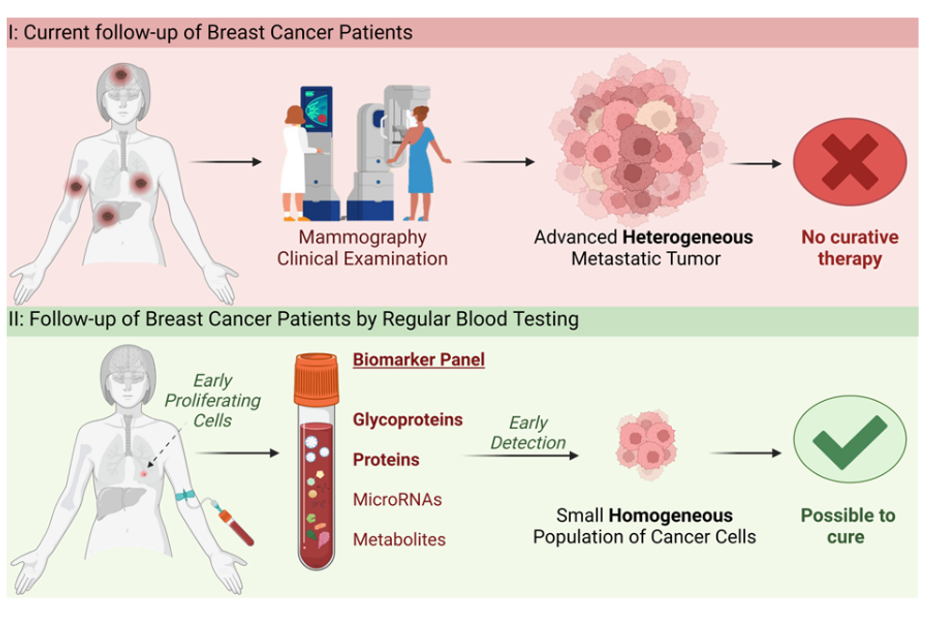
En stor utfordring med brystkreft er risikoen for tilbakefall, som kan skje mange år etter behandling. Den største utfordringen er systemiske tilbakefall, dvs. når kreften sprer seg til andre organer i kroppen. I dag mangler vi gode metoder for å oppdage dette tidlig, og sykdommen blir ofte først oppdaget når en ny svulst gir symptomer eller synes på radiologiske undersøkelser. Når tilbakefall oppdages så sent, er behandling med mål om å bli frisk som regel ikke mulig, og pasienten må over på livsforlengende behandling i stedet.
For å gi pasientene bedre trygghet, trenger vi metoder som kan oppdage tilbakefall lenge før dagens undersøkelser. I prosjektet vårt analyserer vi blodprøver for proteiner, glykoproteiner, metabolitter og mikro-RNA. Ved å sammenligne prøver fra pasienter med og uten tilbakefall, samt friske kontroller, håper vi å finne markører som kan avsløre tidlige tegn på tilbakefall og gi mulighet for tettere og mer personlig oppfølging. Arbeidet utføres av PhD student Marie Landa Austbø ved Avdeling for patologi, Stavanger Universitetssykehus.
Delprosjekt 3: Flytende biopsier for persontilpasset oppfølging av pasienter med opererbar brystkreft
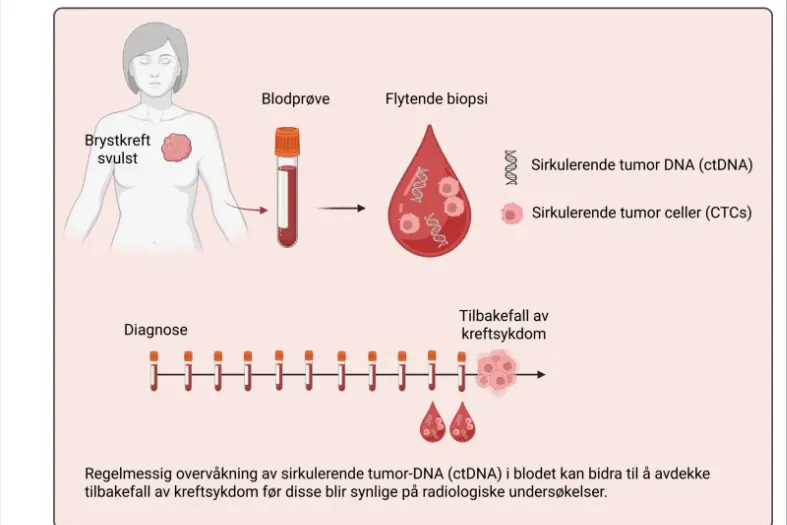
Bildet viser at regelmessig overvåkning av sirkulerence tumor DNA (ctDNA) i blodet kan bidra til å avdekke tilbakefall av kreftsykdom før disse blir synlige på radiologiske undersøkelser.
Sirkulerende tumorceller i blod er vist å ha betydning for prognosen til brystkreftpasienter. Den konvensjonelle metoden for å påvise disse kreftcellene (CellSearch) er avhengig av overflateproteinet EpCAM, som er nedregulert i en del sirkulerende tumorceller som følge av en epithelial-til-mesenkymal celleforandring. Vi vil i denne studien undersøke nytteverdien av å påvise alle typer kreftceller i blodet uavhengig av om de har overflateproteinet EpCAM til stede, ved tidlig brystkreft.
Tumorcellene opp-konsentreres ved hjelp av den immunomagnetiske metoden MINDEC (som vi selv har utviklet) og påvises ved kvantitativ RT-PCR ved måling av mRNA-markører som er nærmest fraværende i normale blodceller, men til stede i kreftcellene.
Blodprøver tatt før operasjon blir undersøkt med tanke på å kunne forutsi prognose. Halvårlige blodprøver etter operasjon utgjør et unikt materiale for å evaluere verdien til undersøkelsene i forhold til sykdomsovervåkning.
Sirkulerende tumor DNA (ctDNA) er en annen lovende biomarkør for prognose og sykdomsutvikling ved brystkreft. ctDNA har sitt opphav i døende celler fra brystkreftsvulsten, eller eventuelle metastaser, og kan påvises ved hjelp av tumorspesifikke mutasjoner. I denne studien vil vi påvise og karakterisere ctDNA ved hjelp av neste-generasjons sekvensering (NGS), der plasma prøver tatt før operasjon samt halvårlige oppfølgingsprøver fra pasienter i PBCB studien vil bli analysert. Nivået av ctDNA, gjennom en eventuell økning i forekomst av spesifikke mutasjoner, vil bli sammenholdt med røntgenbilder for overvåking av sykdommen. På den måten kan vi både avdekke om måling av ctDNA har en klinisk betydning og avdekke eventuelle resistensmutasjoner dersom pasientene får kjemoterapi. Arbeidet utføres av PhD student Kristin Løge Aanestad fra Forskningsgruppe for kreft og medisinsk fysikk, Mikrometastasegruppen, Stavanger Universitetssykehus.
Fatigue hos brystkreftoverlevere
Nye behandlingsmetoder og tidlig oppdagelse gjør at flere overlever brystkreftsykdommen, men mange overlevere sliter med senskader fra behandlingen. Opptil 30-40% av kvinnene rammes av fatigue (sykelig/kronisk utmattelse, slik at de har vankeligheter med å komme tilbake til arbeid. Tross den betydelige kostnaden for både pasient og samfunn, vet man lite om sammenhengen mellom brystkreft, kreftbehandling og slike senskader. Mekanismer for hvordan fatigue rammer noen kraftig, mens andre ikke, er også svært begrenset.
PBCB materialet er godt egnet til studier der mekanismer for vedvarende fatigue studeres, siden longitudinelle kliniske-, biologiske- og PROM-data kan trianguleres sammen.
REsearch on BrEast Cancer induced chronic conditions supported by Causal Analysis of multi-source data (REBECCA).
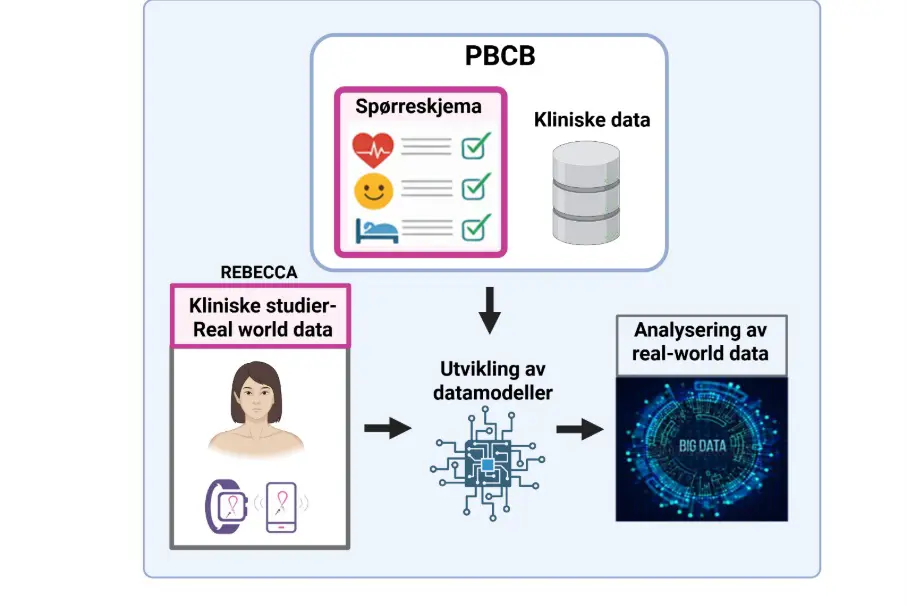
Bildet viser en oversikt over bruken av PBCB data i REBECCA EU prosjektet
Kreftrelatert fatigue er en av de vanligste senbivirkningene etter brystkreft behandling, og kan vedvare i flere år hos ellers friske overlevere. Fatigue er en kompleks, multidimensjonal tilstand som påvirker pasientene fysisk, mentalt og emosjonelt, og har derfor for enkelte pasienter betydelig innvirkning på generell funksjonsevne, livskvalitet og arbeidsevne. Kreftoverlevere som rammes av fatigue kan derfor oppleve økt økonomisk belastning og stress, og har et høyere forbruk av helsetjenester.
I dag får helsepersonell innsikt i pasientenes livskvalitet hovedsakelig gjennom spørreskjemaer (PROMs). Disse spørreskjemaene baserer seg på pasientenes subjektive vurderinger, hvor oppfatningen av fatigue kan variere betydelig. SUS deltok derfor som eneste norske institusjon i et EU-finansiert prosjekt hvor man vil kartlegge livskvaliteten hos brystkreftoverlevere rammet av senbivirkninger som blant annet kreftrelatert fatigue gjennom innsamling av objektive livstilsdata. Såkalte “real-world data” ble da samlet inn gjennom bruk av smartklokker og en REBECCA mobil app i tre kliniske REBECCA studier ved SUS. I denne sammenhengen ble også spørreskjemaene og kliniske data samlet inn i PBCB analysert for å studere sammenhenger mellom ulike parametere og fatigue status (resultater ikke publisert). Denne innsikten danner videre grunnlag for utvikling av datamodeller som analyserer «real-world data» fra REBECCA-prosjektet. Figuren ovenfor viser en oversikt over REBECCA EU-prosjektet, hvor analyser av PBCB-dataene inngår. Home - REBECCA
Østrogennivåer ved langtidsbehandling med aromatasehemmere
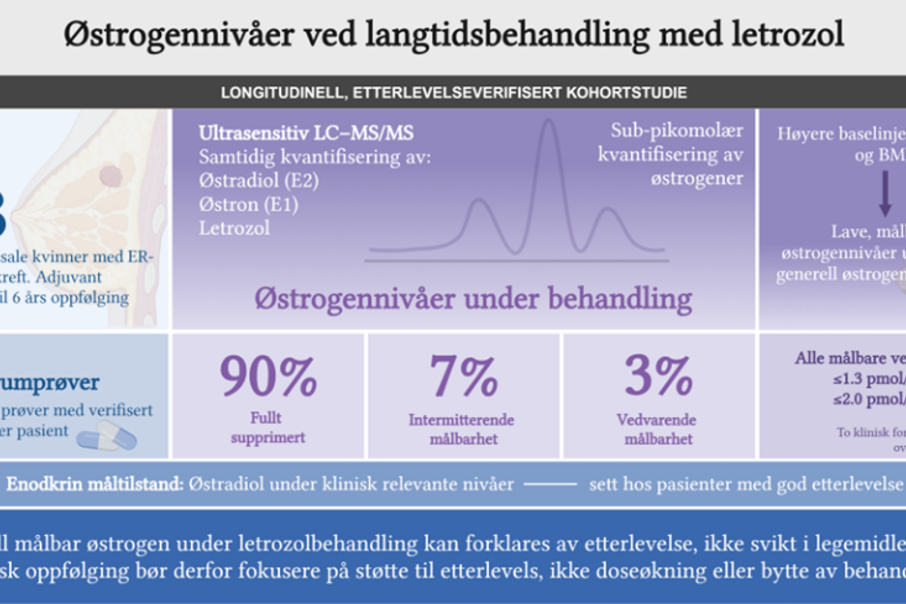
Bildet viser en oversikt over prosjektet.
Aromatasehemmere er blant de mest brukte kreftlegemidlene i verden og er helt sentrale i behandlingen av østrogen-reseptor positiv brystkreft hos post-menopausale kvinner. Legemidlene virker ved å blokkere enzymet aromatase, som omdanner androgener til østrogen i kroppens ved, særlig i fettvev.
Flere studier har rapportert målbare østrogennivåer hos enkelte pasienter under behandling. Dette har reist spørsmål om hvorvidt aromatase-hemmere alltid gir tilstrekkelig østrogensuppresjon, særlig hos kvinner med høy kroppsmasseindeks. Tidligere studier har imidlertid hatt begrenset oppfølgingstid, manglet verifikasjon av legemiddeleksponering og benyttet analysemetoder uten tilstrekkelig følsomhet.
I dette prosjektet har vi brukt PBCB til å følge 228 postmenopausale kvinner behandlet med letrozol, med 1154 serumprøver samlet inn gjennom opptil seks år. Ved hjelp av ultrasensitive massespektrometriske metoder har vi målt østradiol, østron og letrozol, der letrozolnivåene gir en objektiv verifikasjon av behandlings-etterlevelse (adherence).
Studien viser at letrozol gir en robust og vedvarende østrogensuppresjon. Nitti prosent av pasientene var fullt supprimert ved alle måletidspunkter, og kun et lite mindretall hadde vedvarende målbare østrogennivåer. Det ble ikke observert biokjemisk «escape» eller gradvis økning i østrogener over tid. Kvinner med høy kroppsmasseindeks og høyere østrogennivåer før behandlingsstart hadde noe oftere lave, målbare verdier, men uten tegn til klinisk relevant svikt i suppresjonen.
Samlet indikerer funnene at ufullstendig østrogensuppresjon i stor grad reflekterer redusert etterlevelse snarere enn utilstrekkelig legemiddeleffekt. Klinisk oppfølging bør derfor prioritere verifikasjon og støtte av behandlingsetterlevelse, ikke doseeskalering eller bytte av endokrin behandling.
PROTAM: Endokrine effekter av tamoksifenbehandling
Tamoksifen er et endokrint legemiddel med en kompleks og vevsspesifikk virkningsprofil i brystkreftbehandling. Legemidlet virker primært ved å blokkere østrogenreseptoren i brystvev, men utøver både agonistiske og antagonistiske effekter i andre vev. Til tross for omfattende klinisk bruk er tamoksifens påvirkning på det systemiske hormonmiljøet fortsatt mangelfullt kartlagt.
Flere studier har rapportert såkalte off-target-effekter av tamoksifen, og nyere forskning har fremhevet betydningen av samspillet mellom østrogen-, progesteron- og androgenreseptorer i brystkreftbiologi. Tidligere undersøkelser av hormonelle endringer under tamoksifenbehandling har imidlertid vært begrenset av små pasientmaterialer, analysemetoder med utilstrekkelig sensitivitet og analyser hovedsakelig på gruppenivå.
PROTAM (SteroidPROfilering av TAMoxifen) er et forskningsprosjekt som undersøker hvordan tamoksifenbehandling påvirker det systemiske steroidhormonmiljøet hos både pre- og postmenopausale brystkreftpasienter. Ved å analysere serumprøver før og under behandling kartlegger vi individuelle hormonelle endringer og påvirkning av sentrale endokrine akser over tid. Prøvene analyseres med massespektrometriske metoder som samlet dekker store deler av steroidsyntesen og muliggjør detaljert hormonprofilering på et nivå som tidligere ikke har vært mulig. Så langt er 350 serumprøver fra PBCB klargjort for analyse.
Resultatene kan gi ny innsikt i de systemiske endokrine effektene av tamoksifenbehandling og bidra til å belyse hormonelle endringer med relevans for bivirkninger og individuell variasjon i behandlingsrespons.
|
PhD kandidat |
Veiledere |
Tittel |
Status |
|
Thomas Helland, molekylærbiolog |
Gunnar Mellgren, Håvard Søiland, Emiel Janssen |
Tamoxifen i behandling av luminal brystkreft - Implikasjoner av aktive metabolitter for genuttrykk, bivirkninger og klinisk utfall. |
Disputert 22.02.2019 |
|
Kari Britt Hagen, sykepleier |
Ragna Lind, Håvard Søiland |
Brystkreft: Etterlevelse av adjuvant endokrin behandling hos pasienter i Vest-Norge, |
Disputert 23.09.2019 |
|
Finn Magnus Eliassen, overlege |
Gunnar Mellgren, Tone Hoel Lende, Thomas Helland |
Betydning av adherence for klinisk utfall hos pasienter med brystkreft som får adjuvant endokrin behandling |
PhD prosjekt startet |
|
Marie Austdal, molekylærbiolog |
Emiel Janssen |
Persontilpasset monitorering av brystkreft (PerMoBreCan) |
Post doc. prosjekt ferdig |
|
Marie Landa Austbø, molekylærbiolog |
Emiel Janssen |
Validering av nye biomarkører for påvisning av tidlig tilbakefall hos brystkreftpasienter |
PhD prosjekt startet |
|
Kristin Løge Aanestad, lege |
Bjørnar Gilje, Oddmund Nordgård og Kjersti Tjensvoll |
Flytende biopsier for persontilpasset oppfølging av pasienter med opererbar brystkreft
|
PhD prosjekt startet |